Первая научная статья об ЭпиВакКороне. Часть 1
 prof_afv — 01.04.2021
prof_afv — 01.04.2021
Долгожданная научная публикация о вакцине ЭпиВакКорона наконец появилась: https://www.rospotrebnadzor.ru/files/news/1699-10615-2-PB.pdf. Статья посвящена предварительным результатам Фазы 1-2 клинических испытаний, которые пока ещё не закончены. Начну с главного – к сожалению, многие важные научные вопросы остались без удовлетворительного ответа. Меньше всего вопросов относительно развития нежелательных явления (НЯ) после вакцинации. Судя по данным статьи, краткосрочные НЯ у вакцинированных отмечались редко и были лёгкими. Правда, количество вакцинированных было невелико – 57 человек, т.е. НЯ с частотой менее 1:100 в этом исследовании выявлены быть не могли. Тем не менее, похоже, что вакцина ЭпиВакКорона действительно низко реактогенна. А вот вопросов по иммунногенности этой вакцины много и однозначного ответа на них статья не даёт. Поскольку речь идёт о фазе 1-2 клинических испытаний, то определение протективной эффективности на этом этапе было невозможно. Так что вопрос о протективности ЭпиВакКороны остаётся открытым, несмотря на то, что эта вакцина уже несколько месяцев находится в гражданском обороте.
Теперь о статье конкретно. Будет скучновато, придётся вникать в детали. А в них, как известно, бес кроется. Много раз повторял, но так-как этот пост на «горячую тему», повторю ещё раз – я выражаю только своё мнение (подробнее об этом в авторской декларации – см. верхний пост).
Выбор журнала
Статья опубликована в журнале «Инфекция и Иммунитет» (Infection and Immunity), который издаётся Институтом им. Пастера, Санкт-Петербург, ведомственно подчинённым Роспотребнадзору. Назвать этот журнал международным можно, но с большой натяжкой. Он явно не относится к журналам, активно читаемым в международном научном сообществе. Импакт-фактор этого журнала очень низкий (0,6-0,7). Для тех, кто не в курсе – импакт-фактор это наукометрический показатель, характеризующий среднее количество цитирований в течение предшествующего года на одну статью, опубликованную в этом журнале. У импакт-фактора есть немало недостатков. Это отдельная тема. Его нельзя использовать для оценки каждой статьи, опубликованной в журнале. Иными словами, в журналах с высоким импакт-фактором может «проскочить» статья не самого высокого научного качества, а в журнале с низким импакт-фактором может быть опубликована хорошая научная статья. Но это исключения. В целом же, величина импакт-фактора и рейтинг журнала в своей категории (что более информативно) дают представление об уровне журнала и степени строгости осуществляемой в нём научной экспертизы рукописей. Поэтому для профессионалов важно в каком журнале опубликована статья. Хорошей иллюстрацией этому является изменение отношения к Спутнику V после двух публикаций в Ланцете (импакт-фактор Ланцета – 60,4).
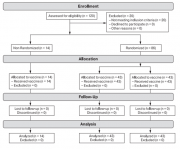
Ну, хорошо, может быть эта статья исключение. Хотел бы, чтобы это было так. Но, увы, даже поверхностное ознакомление со статьёй обнаруживает «ляпы», которые должны были быть исключены в процессе подготовки рукописи (у статьи 23 автора, которые, по идее, должны были её прочитать), в ходе профессионального рецензирования при рассмотрении рукописи в журнале (должно быть минимум 2 рецензента, специалистов в этой области) и, наконец, в процессе технического редактирования статьи. Перечислять всё не буду, но вот несколько примеров. Ниже таблица, очень важная для статей, описывающих клинические испытания. В ней, в формате flow-chart представлена информация о том, как были сформированы группы.

Попробуйте найти группу плацебо. Её нет. Зато много ненужной информации (всё, где n=0). А вот важная информация о том, что группы «вакцина» Фазы 1 (n=14) и Фазы 2 (n=43) были объединены и рассматриваются в статье как одна группа (n=57), в этой диаграмме нет.
Другой пример – описание титрования сывороток испытуемых для тестирования в ИФА (стр 288). Там вообще не о людях а о животных:

Понятно, что это ошибка, возникшая в результате копирования в рукопись фрагментов других текстов. Такое бывает. Но как это могли пропустить все авторы, рецензенты и редакторы? И далее одно тянет другое. Скажем, в этом фрагменте написано, что первым тестируемым разведением сывороток было 1:40 (обратный титр 40). А если посмотреть на данные в соответствующей таблице (таблица 3, стр. 293), то получается, что в одних случаях первым разведение было 1:40, а в других 1:50. То есть ряд титрования для одних сывороток (в обратных титрах был) 40-80-160-320 и т.д., а для других 50-100-200-400 и т.д.?
Список «шероховатостей» можно продолжить, но тогда пост станет ещё более длинным и специальным. Поэтому перейду к более смысловым моментам. Но, вынужден отметить, что неряшливость оформления работы и низкий уровень её научного рецензирования создают неблагоприятный фон.
Какова «рецептура» ЭпиВакКорона?
Ответа на этот вопрос статья не даёт, что к её достоинствам явно не относится. Наверное, многим в голову приходит аргумент, что это «секрет фирмы». Если так, то это секрет Полишинеля. Вся информация о структуре пептидов и белке-носителе дана в патенте RU 2743595. Текст патента свободно доступен. Какой смысл опускать эту информацию в статье на английском языке, предположительно ориентированной на международное научное сообщество? А в статье это было бы очень кстати, как для того, чтобы яснее представить результаты, так и для обсуждения многочисленных вопросов, которые возникают в связи с этими элементами конструкции вакцины.
ЭпиВакКорона состоит из белка-носителя и 3 пептидов. Пептиды ковалентно «прицеплены» к белку-носителю, каждый индивидуально. Иными словами, вакцина это смесь равного количества трёх компонентов, каждый из которых это один и тот же белок-носитель с «привязанным» к нему одним из следующих пептидов:

Область белка S, в которой находятся эти пептиды, указана в колонке справа (RBD и HR2). Первая аминокислота каждого пептида - цистеин (С). Эта аминокислота «добавочная», её нет в аминокислотной последовательности белка S. Введена она в пептид для того, чтобы «привязать» его к белку-носителю. Эта химическая процедура широко применяется для получения комплексов белок-пептид. Интересно, что пептиды 2 и 3 находятся в одной и той же зоне S-белка и существенно перекрываются (перекрёст 12 аминокислот, выделен голубым). В чем логика такого выбора пептидов из статьи не ясно.
Белок-носитель в ЭпиВакКорона необычный. Обычно для этого используют бычий сывороточный альбумин (BSA) или гемоцианин лимфы улитки (KLH). А в ЭпиВакКороне использован химерный бактериальный белок, в котором слиты воедино бактериальный белок MBP и коронавирусный белок N, плюс «довесок» - цепочка из 6-ти гистидинов. Довесок этот введён в состав белка-носителя с чисто технологической целью – он необходим для его очистки от других бактериальных белков с помощью широко используемого для этого варианта аффинной хроматографии. В принципе этот гистидиновый довесок было бы лучше удалить, но это усложняет технологию наработки белка-носителя и разработчики ЭпиВакКороны решили этого не делать. На рисунке ниже показана первичная структура белка-носителя ЭпиВакКороны. Серый фрагмент это собственно бактериальный белок (МBP - белок, связывающий мальтозу), голубой фрагмент это белок N SARS-CoV-2, кроме двух первых аминокислот обозначенных сиреневым.

Все природные белки начинаются с метионина - M (но пост-трансляционные модификации это могут изменить). В химерном белке «N часть» пристыкована к хвосту «MBP части». В такой ситуации «первый” M не нужен. Поэтому вместо M стоит L. Почему заменена вторая аминокислота, не знаю. Наверное, это как-то обосновано технологически. Но, в принципе, это не очень важно. Значительно важнее то, что химерный белок продуцируется бактерией - кишечной палочкой. Это означает, что его гликозилирование (присоединение сахаров к некоторым аминокислотам) происходит иначе, чем в клетках человека, других млекопитающих и вообще эукариотических клетках. А это меняет антигенность белка. Другое неизвестное – это конформация, которую принимает N-белок, когда он «сцеплен» с MBP белком. Оптимистическое предположение, что в этом случае его конформация такая же, как и у природного белка N. Но это не гарантировано. Следующее неизвестное это степень «нагруженности» гибридного белка-носителя пептидами. Ведь «прицепленные» пептиды могут экранировать естественные эпитопы белка-носителя, тем сильнее, чем больше их с белком «сшито». Информация, относящаяся к оценке этих важных параметров, в статье отсутствует.
Последним элементом рецептуры является адъювант. Он традиционный – гидроокись алюминия, которая используется в вакцинах с конца 20-х годов прошлого века.
Какие есть основания предполагать, что эпитопы белков S и N SARS-CoV-2, включенные в ЭпиВакКорону, способны индуцировать протективный иммунный ответ?
Данные, представленные в статье, таких оснований почти не дают. Правда, в статье сообщается о выработке у вакцинированных нейтрализующих антител. Но данные по нейтрализующим антителам не содержат важных деталей, без которых трудно судить об их надёжности (подробнее об этом будет в Части 2). Помимо этого, сравнение локализации пептидов ЭпиВакКорона с локализацией известных линейных B-эпитопов S-белка обнаруживает несовпадение – пептиды ЭпиВакКороны находятся в низкоиммуногенных областях белка S. Что касается белка N, то эпитопов, вызывающих выработку нейтрадизующих антител, в нём нет. А вот Т-эпитопы есть и в значительно большем количестве, чем у белка S. Но, к сожалению, информация о Т-клеточных ответах, индуцируемых вакциной ЭпиВакКорона, в статье полностью отсутствует.
Так на чем же основывается предположение о протективной эффективности ЭпиВакКороны? Пока это только результаты экспериментов на животных, на которые авторы ссылаются в статье. Но, во-первых, эти результаты в виде научной статьи остаются неопубликованными, а во-вторых, к сожалению, результаты доклинических испытаний вакцин далеко не всегда воспроизводятся в клинических испытаниях.
Пост уже очень длинный. Продолжение в Части 2, в которой я остановлюсь более подробно на данных по иммуногенности ЭпиВакКороны.
Проф_АФВ

 Как выбрать смартфон для создания идеального контента в социальных сетях
Как выбрать смартфон для создания идеального контента в социальных сетях  Хорошая ли ты хозяйка?! Тест времен СССР
Хорошая ли ты хозяйка?! Тест времен СССР  Геометрическая задача
Геометрическая задача  совсем нет гнили
совсем нет гнили  Как в 1991-м уговаривали украинцев голосовать против Союза, или Как Украина
Как в 1991-м уговаривали украинцев голосовать против Союза, или Как Украина  Тайский ресторанчик
Тайский ресторанчик  Немного о "бедных несчастных мирных" газаватах...
Немного о "бедных несчастных мирных" газаватах...  Азовская кольцевая
Азовская кольцевая  Кэролин Врилэнд на фотографиях из Instagram
Кэролин Врилэнд на фотографиях из Instagram 





